À écouter certains, il suffirait de promouvoir l’innovation pour que nous puissions tous circuler en voiture électrique ou à hydrogène sans émettre de CO2. Mais est-ce vraiment aussi simple ?
« Rien ne se perd, rien ne se crée, tout se transforme. » Cette citation, souvent attribuée au chimiste du XVIIIᵉ siècle Antoine Lavoisier, résume bien les principes de la thermodynamique, qui étudie les transformations de la matière et les conversions d’une forme d’énergie à une autre.
Nous fêtons en 2024 le 200e anniversaire d’une des œuvres fondatrice de cette discipline : « Réflexions sur la puissance motrice du feu », par Sadi Carnot. C’est lui qui a le premier compris que si l’énergie ne se perd pas (premier principe), elle se détériore de manière irrémédiable (second principe).
Autrement dit, la thermodynamique fixe le cadre de ce qui est physiquement possible ou non en matière d’énergie. C’est à cause d’elle que les voitures volantes promises par la science-fiction ne volent toujours pas au-dessus de nos têtes…
On y distingue deux grandes branches :
- la première décrit le rendement maximal pour chaque transformation de la matière ou conversion d’énergie ;
- la seconde décrit les propriétés de la matière à l’équilibre.
Aujourd’hui encore, comprendre les lois de la thermodynamique reste crucial si l’on souhaite élaborer des propositions réalistes en matière de transition énergétique et écologique.
Comprendre ce qu’est l’énergie grâce à la thermodynamique
Dans la pratique, lorsque nous utilisons une énergie, nous la transformons. Nous ne pouvons pas la détruire, en vertu du premier principe de la thermodynamique, qui établit que lors de toute transformation, il y a conservation de l’énergie. Peut-elle donc être réutilisée ? Ce serait bien utile pour un monde renouvelable.
Malheureusement, non, car nous la dégradons, en vertu du second principe de la thermodynamique, qui établit l’irréversibilité des phénomènes physiques. En transformant l’énergie, nous créons ce que nous appelons de l’entropie.
En quelque sorte, l’énergie perd de sa valeur : on peut faire moins de choses avec. L’exemple le plus connu concerne la chaleur. À haute température, il est possible de la transformer en électricité (par exemple à l’aide d’une turbine à vapeur), alors qu’à basse température, cette même énergie ne peut plus servir qu’à nous chauffer. La « valeur » de l’énergie peut être quantifiée sous une grandeur appelée « exergie ».
La matière aussi peut perdre de sa « valeur », par exemple lorsqu’elle est mélangée : il est préférable d’avoir de l’eau pure que de l’eau sale, par exemple.

Sur le schéma, on distingue les flux d’énergie (par exemple chaleur, énergie électromagnétique, énergie cinétique…) et les flux de matière.
L’exergie sert de monnaie d’échange entre ces deux flux : on peut par exemple chauffer de la matière pour stocker de l’énergie, ou la refroidir pour déstocker. On peut également utiliser de l’énergie pour purifier des mélanges (par exemple, dessaler de l’eau de mer) ou pour transformer un produit en un autre (par exemple fabriquer de l’hydrogène par électrolyse de l’eau). Inversement, la matière peut aussi nous fournir de l’énergie : par exemple, un carburant qui va réagir avec l’air pour produire de la chaleur – mais aussi du dioxyde de carbone (CO2).
L’épaisseur des flèches ne représente donc pas la masse (qui, elle, ne change pas), mais bien l’exergie. Malheureusement, quel que soit le procédé de transformation – qu’il s’agisse de celles de l’industrie ou de la vie elle-même – il y aura une perte d’exergie. Tout retour en arrière est impossible !
L’exergie fournit en quelque sorte une échelle de valeur. En effet, certains produits contiennent naturellement une grande quantité d’exergie (par exemple les hydrocarbures, mais également l’hydrogène), d’autres au contraire en sont pauvrement dotées (le CO2 ou l’eau). Vouloir les transformer en autre chose implique forcément un apport d’énergie conséquent.
L’enjeu du stockage de l’énergie
Dans le contexte de la transition énergétique, l’intermittence liée aux énergies renouvelables est une contrainte. C’est le grand inconvénient du vecteur électricité : aussitôt produit, il faudra le consommer… ou le stocker. Ceci peut se faire par bien des moyens. Par exemple de manière mécanique (station de pompage pour l’énergie hydraulique ou volants d’inertie), thermique (réservoirs à haute température) ou encore chimique. Le cas d’usage le plus connu est celui des batteries, même si on parle aujourd’hui aussi beaucoup de l’hydrogène.
Ces réservoirs de matière riche en énergie pourront ensuite être exploités pour récupérer de l’exergie en utilisant un procédé inverse. Or, comme on l’a vu, il y a des pertes : à chaque étape, la quantité d’exergie diminue.
Pour réussir la transition énergétique, il est donc non seulement nécessaire de travailler sur l’efficacité (le rendement) de ces transformations (diminuer les pertes), mais également d’en limiter le nombre total.
Alors que nos ancêtres utilisaient la force du vent pour faire tourner leurs moulins, nous transformons désormais l’énergie éolienne en électricité dans des turbines (rendement de 65 %) pour ensuite produire de l’hydrogène (rendement de 70 %) qui sera ensuite introduit dans un moteur à combustion interne (rendement de 45 %) pour fournir de l’énergie mécanique. Le rendement total est le produit de tous les rendements de la chaîne de transformation : soit, dans notre exemple, d’environ 20 %…
De ces quelques réflexions, on pourra conclure que l’hydrogène, sauf à en trouver des sources naturelles, sera toujours cher à produire. De même, chercher à valoriser le CO2 (pour le stocker par exemple) consommera toujours beaucoup d’énergie.
Les propriétés de la matière, clé de la transition écologique
L’application du second principe de la thermodynamique (irréversibilité des transformations) implique que naturellement, l’entropie d’un système est maximale lorsqu’il est à l’état d’équilibre. Sans rentrer dans tous les détails techniques, cela correspond également au minimum d’une autre grandeur que nous appelons l’enthalpie libre de Gibbs.
À condition d’avoir un modèle qui décrit comment l’enthalpie libre évolue en fonction des conformations de la matière, cela permet d’en déduire le comportement naturel spontané des molécules. On parle de thermodynamique chimique.
Cette approche nous permet de calculer quelle est la température à laquelle un solide se transforme en liquide puis en vapeur, en fonction de la pression ambiante. Ou encore, à partir de quelle concentration un solide sera saturé dans une solution, par exemple, la saturation en sel ou en sucre de l’eau).
De manière imagée, et avec l’aide des autres sciences, on pourra construire ce qu’on pourra appeler en chimie le « paysage énergétique » d’un système à l’équilibre. Ce paysage décrit la stabilité d’un système matériel en fonction des variables comme la température, la pression ou la composition.
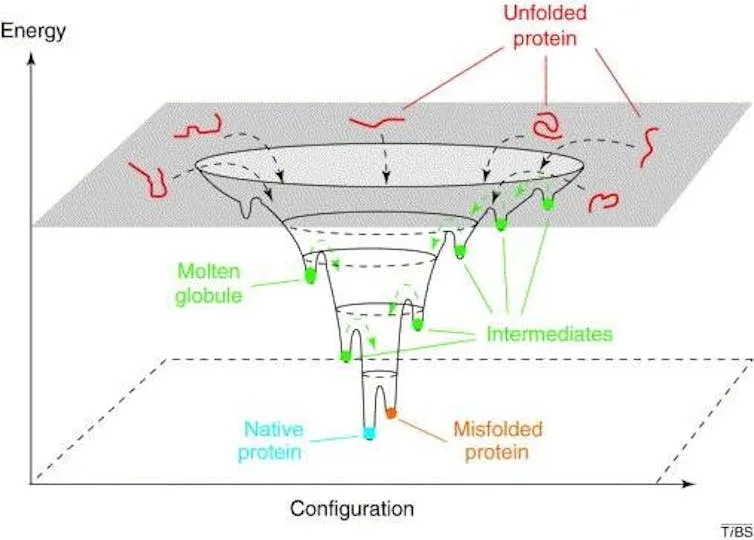
Naturellement, le système va tendre vers l’enthalpie libre la plus faible possible. Cependant, il peut se coincer dans un état dit métastable (ce qui correspond à un minimum local, en vert sur l’illustration ci-dessus), ce qui peut être désiré ou non. Dans ce dernier cas, on pourra éventuellement le « pousser » pour l’aider à passer dans un état plus fondamental (en bleu).
Ces paysages permettent de décrire les configurations possibles de la matière dans toutes sortes de conditions (pression, température, apport d’énergie…). Ils nous permettent aussi de choisir des chemins optimaux, en partant de matières premières données pour arriver à un produit désiré, en minimisant l’énergie nécessaire ainsi que la production de déchets.
Ces enjeux sont cruciaux tant pour la transition énergétique que pour la transition environnementale. Que ce soit pour purifier l’eau, nourrir la population, la soigner, la loger ou produire des biens de consommation recyclables, la thermodynamique propose de nombreux outils, ainsi que de nombreux défis : la construction de modèles est une affaire complexe qui demande des spécialistes de bon niveau.
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l'article original.

